die Zukunft – Unsere Plattformtechnologie.
Wir leben Biotech
Die Natur bietet Lösungen für nahezu alle Probleme – diese Prozesse gilt es, für uns Menschen nutzbar zu machen. Das ist Biotechnologie, die Industrie der Zukunft: wahrhaft nachhaltig, klimaneutral und ein Garant für unseren Lebensstandard.
Der Schlüssel zum Erfolg sind effiziente Enzyme, die natürlichen Katalysatoren. Deswegen optimieren wir als Protein-Ingenieure Enzyme für die Anwendung und erschaffen so neue Medikamente durch kontrollierte Biosynthese.
die grundlage.
Naturstoff: Polyketide
Die Evolution hat unzählige biologisch-aktive Substanzen hervorgebracht – sogenannte Naturstoffe. Diese bieten ihren Produzenten große Vorteile gegenüber Fressfeinden oder Konkurrenten und werden insbesondere von Mikroorganismen und Pflanzen durch Biosynthese hergestellt. Die biochemischen Prozesse dahinter sind häufig äußerst komplex und können nur in Ausnahmefällen durch synthetische Verfahren wirtschaftlich rentabel ersetzt werden.
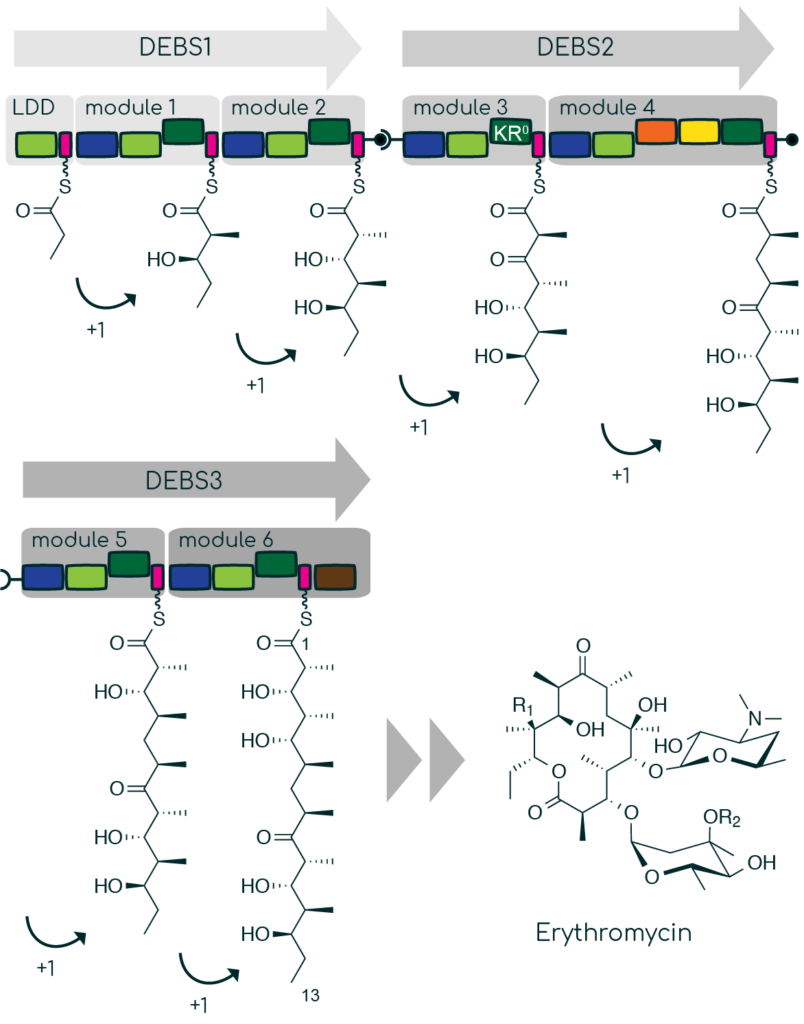
Eine besonders komplexe und strukturell vielfältige Naturstoffklasse sind Polyketide, die eine Anwendung als Wirkstoff in nahezu allen medizinischen Bereichen in Aussicht stellen. Die Biosynthese erfolgt über gigantische Enzymfabriken und gleicht dem Prinzip einer industriellen Fertigungsanlage.
Das Problem.
Wirkstoffe sind nicht gleich Medikamente
Natürlich vorkommende Polyketide können nur in Ausnahmefällen direkt als Medikament verwendet werden, da sich die Bedingungen im Körper grundlegend von denen im natürlichen Umfeld unterscheiden. So sind die Drug-Target Spezifität, physikochemische Eigenschaft, Bioverfügbarkeit, Pharmakokinetik und metabolische Stabilität des Wirkstoffs entscheidende Faktoren, um einen sicheren und nebenwirkungsarmen Einsatz in Patient*innen zu gewährleisten. Um diesen hohen Anforderungen zu entsprechen, müssen die natürlich-vorkommenden Moleküle in den allermeisten Fällen chemisch leicht verändert werden – durch sogenannte Derivatisierung.
Die Derivatisierung von Polyketiden kann auf drei unterschiedliche Arten erfolgen: durch Totalsynthese, Semi-Synthese oder veränderte Biosynthese. Die Totalsynthese durch Chemiker*innen ist sehr aufwendig und quasi nie wirtschaftlich rentabel. Durch Semi-Synthese – also die nachträgliche Veränderung des Naturstoffs – wurden bisher die meisten Medikamente entwickelt. Sie ist aber sehr zeitaufwendig und bietet nur eingeschränkte Möglichkeiten. Um diese Probleme zu überwinden, müssen Modifikationen bereits während der Fertigung des Polyketids durch Anpassung der Biosynthese installiert werden. Auch wenn die Umsetzung äußerst kompliziert ist – die Enzymfabriken sind so komplex wie ihre Produkte – wir ermöglichen damit annähernd grenzenlose Optionen.
Die Revolution.
Unsere Plattformtechnologie
Unsere kezbio-Plattform schließt die Lücke im Grenzbereich zwischen synthetischer Chemie und Biosynthese und bietet nie dagewesene Optionen zur Modifikation des Polyketid-Gerüsts. Wir setzen direkt in der Biosynthese der Polyketide an und verändern die Enzymfabriken gezielt durch Protein-Engineering. Dabei modulieren wir Proteinarchitektur und Enzymkinetik und erschließen neue Biokatalyseprozesse, die im Genom des Produktionsstamms verankert werden. Dieser kann dann im Labor- oder Industriemaßstab kultiviert werden und produziert dauerhaft und nachhaltig den optimierten Polyketidwirkstoff.
Wir verknüpfen mit unserem Verfahren auf revolutionäre Weise gut etablierte Methoden der Organischen Chemie, Molekularbiologie und Fermentationstechnik mit modernsten Verfahren des Genome-Editings, Bioinformatics und Machine-Learnings. Diese Kombination ist einmalig und ermöglicht es uns, neue Wege an der Grenze zum Unbekannten zu gehen.
die Vorteile.
Wir bieten…
Kurze Entwicklungszyklen
Schnelle Resultate aus dem Bioreaktor ohne langwierige Reaktionsschritt-Optimierungen.
Viele Freiheitsgrade
Der gezielte Austausch von Atomen an einzelnen oder mehreren Positionen erlaubt die Kreation unzähliger Derivate.
Skalierbare Produktion
Ob im Labor- oder Fabrikmaßstab – die mikrobiellen Prozesse lassen sich auf alle Mengenbedürfnisse ohne weitreichende Änderungen anpassen.
Nachhaltige Kultivierung
Unsere Bioreaktoren werden mit nachwachsenden Rohstoffen betrieben, wir streben CO2-Neutralität an.
Günstige Herstellung
Von der Natur optimierte mikrobielle Prozesse statt aufwändige chemische Synthese – wir können die Polyketide zu attraktiven Konditionen produzieren.
Universelle Plattform
Unsere Technologie lässt sich auf alle modularen Polyketidsynthasen und alle Produktionsstämme anwenden.
Unser UsP.
Das KEZ®|Selectase® Paar
Unsere Plattformtechnologie basiert auf einem ausgeklügelten Zusammenspiel zwischen unseren KEZ®-Substraten und der Enzymdomäne MAT. Unser Enzym Selectase® (Patent eingereicht und veröffentlicht) wird molekularbiologisch zielgenau in das Genom des Produktionsstamms eingebracht und bestimmt dadurch die Position der chemischen Modifikation im Polyketidgerüst.
Die KEZ-Substrate werden während der Fermentation beigesetzt und bestimmen die entsprechend gewünschten funktionellen Gruppen. Dabei arbeiten wir kontinuierlich an der Erweiterung der chemisch funktionellen Optionen.
Die Anwendungsbereiche.
Entwicklertool für neue Medikamente
Wir nutzen ausschließlich bereits von der Natur selektierte biologisch-aktive Naturstoffe und bewegen uns im Bereich zwischen Leitstrukturoptimierung, Hit-Validierung und präklinischer Phase der Medikamententwicklung:
Neue Antibiotika
Wir entwickeln den Prototypen für unsere Plattformtechnologie anhand der Biosynthese von Erythromycin, einem sogennanten Makrolidantibiotikum. Diese Wirkstoffklasse zeichnet sich generell durch gute Verträglichkeit aus und unterschiedlichste Vertreter sind seit langem erfolgreich im Einsatz. Wir screenen unsere Wirkstoff-Bibliothek auf Aktivität gegen resistente Keime.
Spezifische Derivate
Das gut erforschte Polyketid zeigt exzellente biologische Aktivität und es existiert ein fundiertes Grundwissen über die Eigenschaften und der Drug-Target Interaktion. Wir installieren gezielt Funktionen an der gewünschten Position, um auf veränderte Target-Strukturen zu reagieren oder die Moleküleigenschaften für die Anwendung zu optimieren.
Wirkstoffbibliotheken
Sind die Zusammenhänge deutlich komplexer oder der Wirkmechanismus des Polyketids noch nicht aufgeklärt, benötigt man für die Weiterentwicklung eine Diversifizierung der Leitstruktur. Wir erstellen mit unserer Plattformtechnologie Wirkstoffbibliotheken, die auf verbesserte Aktivität oder Moleküleigenschaften gescreent werden können.
Building Blocks
Kleine polyketidische Synthons oder Pharmakophore können durch Installation von verschiedenen orthogonalen Gruppen am Gerüst für eine spezifische Weiterverarbeitung vorbereitet werden.